Метод определения содержания свободных аминокислот и амидов в тканях растений
Контроль азотного питания растений может быть проведен несколькими способами: по его валовому содержанию, по количеству нитратов, аммонийного азота, свободных аминокислот и амидов. Последние формы азота особенно необходимо использовать при контроле питания тех групп растений, корневые системы которых характеризуются высокой восстановительной способностью, что исключает возможность контроля их азотного питания по содержанию нитратов в надземных частях. Кроме того, нередки условия существования растений, когда исключается возможность образования нитратов в почве. Известно, что аминокислоты могут накапливаться в тканях как при прогрессивном этапе азотного обмена, так и регрессивном. Поэтому при контроле питания с помощью этих соединений особенно важно убедиться в здоровом состоянии растений — показателе нормального обмена веществ.
При изменении условий питания изменяется не качественный, а количественный состав свободных аминокислот и амидов, причем наибольшие различия получаются у амидов, дикарбоновых аминокислот, пролина, аланина и γ-аминомасляной кислоты, т. е. соединений с низкими Rf. Это позволяет использовать малые хроматограммы. Нами была уточнена и несколько изменена техника хроматографии на малых хроматограммах, предложенная японским ученым Одзаки для аспарагина в листьях риса. Изучением распределения свободных аминокислот и амидов по органам различных растений нами было установлено, что для этого рода диагностики следует использовать самые молодые, не вполне развернувшиеся листья. Было установлено, что у ряда растений при усилении азотного питания увеличивается не только и не столько содержание одного аспарагина, сколько концентрация многих свободных аминокислот и амидов, что и было положено в основу нашего метода.
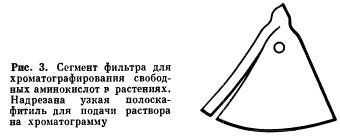
Для хроматографирования использовались круглые беззольные плотные фильтры, которые разрезались на шесть сегментов. С одной стороны каждого сегмента надрезалась узкая полоска-фитиль для подачи растворителя на хроматограмму (рис. 3). Камерами служат чашки Нейбауэра, в центре которых помещают небольшой сосуд с растворителем. Края чашки смазаны вазелином; после размещения в ней хроматограмм камера плотно закрывается стеклом. В каждой камере помещаются четыре хроматограммы: три с испытуемыми пробами и одна с образцовым раствором аминокислот («метчиками»), чем обеспечивается лучшая сравнимость хроматограмм с метчиками, находящимися в одних и тех же условиях. Каждая проба растений испытывалась в шестикратной повторности, причем на сегмент с образцовым раствором в каждую из этих повторностей наносились капли разной концентрации согласно принятой шкале, чтобы сравнить одну и ту же пробу со всей шкалой метчиков. Вид камеры дан на рис. 4.

Проба сока молодых листьев наносится следующим образом. В верхний угол сегмента бумаги, положенного на стекло, выдавливается стеклянным пестиком (d = 0,6 см) сок из пучка листьев (в пучке — 5 самых молодых листочков, а для льна — 10 листочков). Размер пятна сока не должен превышать диаметра пестика, так как только в этом случае будет обеспечено одинаковое количество сока на хроматограмме, равное 9,66 мг +0,82 мг, что установлено специальными замерами и тем подтверждены наблюдения М. А. Белоусова и A.Л. Торопкиной. Пятно образцового раствора наносится аналогичным образом. На каждой хроматограмме простым карандашом ставится номер образца.
Сегменты с пробами сока и образцового раствора помещаются в камеры, полоски-фитили которых опускаются в центральный сосуд с растворителем. Камера закрывается стеклом и оставляется на 4 часа. Предложенный Одзаки одночасовый срок для разгона хроматограммы нами был проверен и была доказана его недостаточность. После высушивания на воздухе хроматограммы проявлялись в термостате при 70° С в течение 20—30 мин. до появления четких окрасок.
Проверка показала, что можно разделить во времени нанесение капель сока листьев на сегмент бумаги и хроматографический анализ аминокислот: после нанесения сока на сегмент бумаги каплю следует быстро высушить (например, «феном»). Таким образом подготовленные пробы могут сохраняться более месяца. Это позволяет в течение лета собрать значительное число проб, которые осенью можно прохроматографировать.
Идентификация аминокислот и амидов проводится путем визуального сравнения размеров и интенсивности окраски пятен на испытуемых и образцовых хроматограммах. Чтобы избежать субъективности в оценке цветов и оттенков пятен, была нами использована «шкала цветов» А.С. Бондарцева.
Связь интенсивности окраски и размера пятна с количеством аминокислот и амидов проверялась на шкале образцовых растворов «метчиков» путем измерения планиметром размеров пятен разных концентраций «метчиков». Сопоставление всех этих данных, а также результаты количественных анализов пятен образцовых растворов на больших хроматограммах позволили дать наряду со шкалой в баллах (табл. 15) количественную характеристику этих баллов (табл. 16).
Содержание свободных аминокислот и амидов в самых молодых листьях зависит от фазы развития (с наступлением репродуктивного развития их количества уменьшаются) и особенностей растения: чем интенсивнее, раньше начинается и более длительно проходит образование новых бутонов (например, у гречихи), тем сильнее и быстрее снижается содержание этих соединений в тканях молодых листьев. Эти выводы получены на основании многократных результатов в опытах с удобрениями разных сельскохозяйственных культур. В качестве примера в табл. 17 приведены данные по наиболее биологически разным трем культурам: льну, овсу и гречихе. I срок — начало бутонизации (у овса — выход в трубку), II срок — цветение. Характеристика оптимального азотного питания по содержанию свободных аминокислот в самых молодых листьях для первых двух фаз развития соответствует данным, приведенным в нижних двух строках табл. 15 при полном обеспечении азотным питанием.

Все аминокислоты и амиды с увеличением концентрации образуют более крупные пятна, главным образом сине-фиолетового или красновато-фиолетового цвета. Аспарагин при высоких концентрациях, а иминокислота пролин при всех концентрациях дают желтый оттенок их пятен на хроматограммах, причем пятна аспарагина при высоких концентрациях становятся оранжевыми.
Реактивы. 1. Растворитель для разгона пятен сока на хроматограммах. 0,2%-ный раствор нингидрина в н-бутиловом спирте и 50%-ной уксусной кислоте при соотношении спирта к кислоте как 2:1.
2. Образцовый раствор аминокислот. Смешанный раствор из следующих аминокислот и амидов: аспарагиновой, глютаминовой, пролина, аспарагина и глютамина. 7,5 мг каждой сухой аминокислоты или амида растворяют в 10 мл 10%-ного изопропилового спирта, подкисленного из расчета 10 мл HCl (уд. вес 1,19) на 1 л спирта. Смешивают по 1 мл каждого раствора аминокислот и амидов в пробирке — рабочий раствор. В угол сегмента микропипеткой наносят точно 1 каплю, содержащую 0,05 мл смеси метчиков, в которой содержится по 7,5 у каждой аминокислоты и амида — это шкала № 1. Шкалу № 2 готовят путем нанесения второй капли на первую после высушивания феном первой. Три капли составят № 3, четыре капли — № 4 и пять капель — № 5.
3. Фильтр «синяя лента» диаметром 15 см. Делится на шесть сегментов.