Значение железа в жизнедеятельности растений (часть 4)
Концентрация избыточного количества активного железа в хлоропластах и других клеточных структурах имеет большое значение для восстановления нормальных уровнен метаболических процессов у облученных растений и животных. Защитное влияние железа, очевидно, связано с явлениями стабилизации молекулярных структур после физиологобиохимических нарушений в очагах поражения.
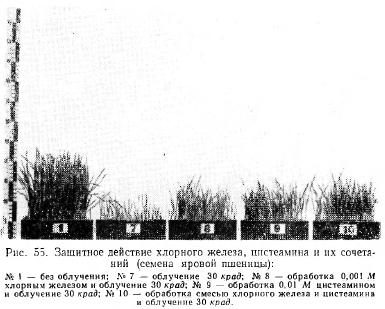
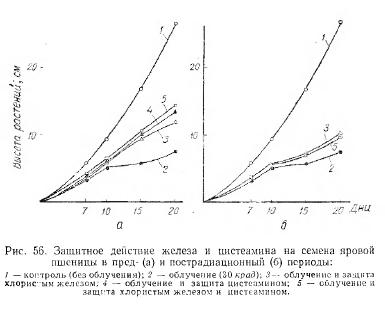
Проведенные нами с Д.М. Гродзинским и И.Н. Гудковым (1966) исследования показали, что двух- и трехвалентное железо, марганец и другие металлы снижают поражающее действие гамма-радиации при использовании их в виде растворов солей как в пред-, так и в пострадиационный период. На рис. 53 и 54 показано защитное действие железа и никеля при облучении семян гороха и яровой пшеницы, а на рис. 55 и 56 степень защитного действия железа сравнивается с действием цистеамина — одного из наиболее эффективных радиопротекторов тиоловой группы. Как видим, действие железа при предрадиационном использовании приближается к действию цистеамина; при совместном же их действии отмечалось явление аддитивности. Однако при пострадиационном введении действие цистеамина в эффекте восстановления не проявлялось. Железо же и в этот период снижало поражающее действие радиации (рис. 56,б).
Как свидетельствуют опыты, проведенные с облученными проростками гороха, защитное действие железа проявляется на протяжении 18—22 час после облучения; действие же тиоловых соединений в весьма незначительной степени ограничивается лишь несколькими часами (рис. 57).
Некоторые металлы, в частности железо и марганец, оказывали значительное защитное действие при облучении проростков кормовых бобов, меристематические клетки которых отличаются чрезвычайно высокой радиочувствительностью (рис. 58). Медь, наоборот, усиливала действие радиации.
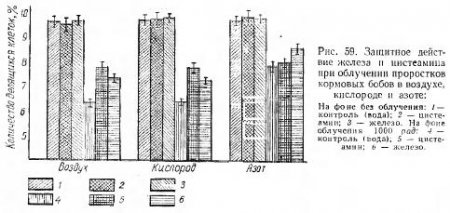
Несомненно, механизм защитного действия железа иной, нежели соединений тиоловой группы. Об этом свидетельствует явление аддитивности, наблюдаемое при совместном использовании этих веществ, а также тот факт, что в отличие от цистеамина защитное действие железа проявлялось также в бескислородной среде (рис. 59). По всей вероятности, механизм защитного действия железа не связан с существованием Кислородного эффекта, уменьшением которого весьма часто объясняется защитный эффект тиоловых соединений.
Вполне возможно, что защитное действие железа и других металлов базируется на способности их к коплексообразованню, с чем может быть связана стабилизация вторичных структур макромолекул (Eichhorn, 1962). В пользу этой гипотезы свидетельствует тот факт, что медь — металл-дестабилизатор, в отличие от других металлов, усиливает действие радиации. Кроме того, как было показано в модельных опытах с растворами ДНК, железо показывает четко выраженное стабилизирующее действие на макромолекулу, благодаря чему сохраняется значительно большее количество хромофорных групп при облучении раствора (рис. 60).
Безусловно, учитывая ту огромную роль, которую играют металлы в жизни живых организмов, можно допустить и ряд иных механизмов, объясняющих их защитное действие при облучении. Возможен механизм, связанный с восстановлением функций металлосодержащих ферментов, изменением проницаемости внутриклеточных мембран, механизм «замораживания» радикалов под влиянием избытка металла и др.
Несмотря на условность проведения параллели между радиобиологическими процессами в клетке и радиационнохимическими реакциями в растворах, все же можно предположить, что в основе защитного действия железа лежат процессы взаимодействия металла с высокополимерными молекулами. Защитное действие железа усиливалось при повышении температуры, что, очевидно, связано с восстановлением системы водородных связей и оструктуренной воды, состояние которых и определяет стабилизацию макромолекулярных образований. Защитное действие железа связано также с образованием комплексных железопорфириновых соединений (гемов) со специфическими белками. В растительных организмах найдены свободные гемотины, которые могут выполнять защитные функции в хлоропластах и в других депо ферментов. Защитная функция железа тесно связана с транспортной, каталитической и оксигеназной функциями гемотинов и гемов и с богатыми энергией фосфатными соединениями АТФ.
Уоллес и Де-Кок (1965) показали, что количество фосфора, поглощаемого и транспортируемого растением, крайне важно для проявления всех функций и гемов и тканей под влиянием железа. При этом фосфор оказывает двойное действие: уменьшает перенос железа к листьям и точкам роста и инактивирует железо в тканях растений. В связи с этим степень снабжения железом, поступление его в ткани зависит от уровня обеспечения растений фосфором (табл. 153).

Защитная, транспортная, каталитическая и другие функции гемотинов и гемов имеют свою специфику у высших растений, грибов и бактерий. Клетки железобактерий и железомарганцебактерий поглощают растворенный бикарбонат закиси железа, окисляют его в своей протоплазме и выделяют окисные соединения железа. Энергия, образовавшаяся при этой экзотермической реакции, превращается в работу, которую клетки железоорганизмов (включая и водорослей) производят при различных своих жизненных отправлениях. По С.Н. Виноградскому, все жизненные процессы этих микроорганизмов совершаются за счет такого своеобразного дыхательного акта.