Метаболические фонды биологических элементов (часть 4)
Используя метод изотопного разбавления, можно получить сведения, позволяющие предположить степень гетерогенности фондов. С этой целью Д.М. Гродзинским (1965) составлены уравнения, с помощью которых можно было рассчитать, как происходит изменение удельной активности продуктов одного предшественника в том случае, когда его фонд гомогенен и гетерогенен. Было выяснено, что при непрерывном введении меченого предшественника удельная активность продуктов с течением времени возрастает по экспоненциальному закону. Удельная активность меченого элемента в продукте постепенно приближается к таковой элемента в предшественнике. В том случае, когда фонд предшественника гомогенен, у всех возникающих из него продуктов удельная активность имеет в пределе одно и то же значение, равное таковой предшественника. При этом время, на протяжении которого удельная активность продукта достигает максимального значения, зависит от скорости реакции. В том же случае, когда фонд предшественника является гетерогенным, для каждого продукта могут быть различными значения удельной активности, если, конечно, удельные активности предшественника в подфондах различны. Отмеченные зависимости показаны на рис. 81. При введении в фонд предшественника меченого вещества таким способом, что перемечивание предшественника в подфондах окажется неравномерным, можно получить кривые, характеризующие изменения удельной активности продуктов с течением времени. Такое определение необходимо делать достаточно быстро после введения меченого предшественника, так как благодаря тому, что подфонды могут быть связаны друг с другом, постепенно начнут сглаживаться различия в их удельных активностях. По начальным точкам можно построить теоретические экспоненты.
Следует отметить, что понятие гетерогенности является условным. Используя обозначения, приведенные на рис. 81, можно говорить о том, что гетерогенность имеет значение в том случае, когда U12 значительно меньше, чем U11 или U22. Следовательно, фонд может быть гомогенным для медленно протекающих реакций и гетерогенным — для быстрых. На рис. 81 также показано схематическое образование продуктов реакций.
В.Н. Ходосом были исследованы изменения удельной активности веществ, образование которых связано с АТФ и ортофосфатом. Для этой цели в листья растений гороха, сахарной свеклы и элодеи вводили меченый ортофосфат и спустя различные промежутки времени определяли удельную активность фосфора, входящего в состав различных фосфорных эфиров и нуклеотидов. Во время экспозиции сохранялись одинаковые условия температуры, освещения и пр., так что должны были иметь место стационарные условия обмена веществ.
Фиксацию растительного материала производили, пользуясь охлажденной трихлоруксусной кислотой. Последнюю отделяли, прибегая к жидкостной экстракции кислоты серным эфиром на холоду. Фосфорные соединения экстракта разделяли с помощью ионообменной хроматографии на Дауэкс-1 по методу Кима и Кона. Этот метод позволяет весьма полно отделять такие фосфорные соединения, как АТФ, АДФ, АМФ, фосфоэнолпируват, 1,6-фруктозодифосфат, глюкозо-1-фосфат и неорганический фосфат. Каждое из этих соединений может быть количественно определено по фосфору либо путем спектрофотометрии. Активность устанавливали с помощью счетчика БФЛ-Т-25 при использовании образцов, содержащих известное количество исследуемого вещества. Все это необходимо было делать для того, чтобы определить коэффициенты обновления отдельных метаболитов. С помощью полученных величин можно было установить характер экспоненциальных зависимостей удельных активностей от времени.
На рис. 82 показаны теоретические экспоненты, полученные при различных экспозициях после внедрения меченого ортофосфата калия в питательную среду, на которой находились растения. Как видим, кривые на графиках очень разные. Очевидно, коэффициенты обновления фосфоэнолпирувата, рассчитываемые по удельной активности фосфора, сильно изменялись на протяжении опыта. Эти данные свидетельствуют о том, что фонд предшественника этого вещества, возможно, гетерогенен. Такие же 5,0 кривые были получены В.Н. Ходосом и для других веществ — АДФ, АТФ и т. п.
Интересно отметить, что условия освещения оказывали сильное влияние па характер изменения коэффициентов обновления веществ. Так, для фосфоэнолпирувата и АДФ на свету скорость обновления уменьшалась, а в темноте, напротив, возрастала. Мы считаем возможным заключить, что скорости изменении удельной активности фосфоэнолпирувата и АДФ испытывают колебания, которые обусловлены гетерогенностью ортофосфата и АТФ.
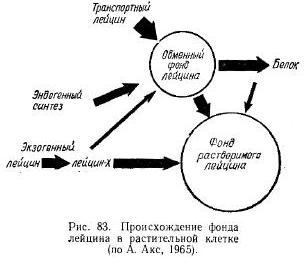
Представления о гетерогенности фонда заставляют с большой осторожностью подходить к оценке кинетики процессов, исследуемых с помощью метода меченых атомов. Это объясняется тем, что при гетерогенности фонда при сравнительно хорошем обеспечении одного подфонда может иметь место недостаточность в другом подфонде. При этом может создаваться своеобразная недостаточность метаболита, хотя па самом деле последний имеется в клетке, но входит в состав разобщенного подфонда. Подобные результаты отмечала, например, А. Акс (Oaks, 1965), изучавшая организацию лейцинового фонда в копчиках корней. Ею установлено (рис. 83), что в корневых окончаниях имеется по крайней мере два фонда лейцина: обменный фонд, который активно участвует в метаболизме, и фонд растворимого лейцина, который легко извлекается из клетки, по практически не участвует в метаболических процессах. Оказалось также, что при введении меченого аланина извне через промежуточное соединение лейцин-Х происходит заполнение фонда растворимого лейцина. Этот фонд слабо связан с обменным фондом в том смысле, что из него лейцин не поступает в фонд аминокислоты, используемой для биосинтеза белка. Пополнение обменного фонда лейцина происходит за счет эндогенного синтеза либо за счет лейцина, проникающего в клетку благодаря передвижению его из других клеток. Лишь очень незначительная часть экзогенного лейцина попадает в обменный фонд. Различие между экзогенным и эндогенным лейцином понять очень трудно, если не признать, что для них имеются разные пути проникновения в растительную клетку.