Определение азота в почве по методу Кьельдаля
Метод состоит из двух операций:
1. Окисление органического вещества почвы серной кислотой при кипячении. Для более быстрого и полного сжигания органического вещества применяют сернокислый калий, повышающий температуру кипения кислоты, и катализаторы: металлический селен и сернокислую медь. Выделяющийся при разложении органического вещества аммиак связывается серной кислотой, образуя сернокислый аммоний.
2. Разложение сернокислого аммония доведением реакции раствора до сильнощелочной, прибавлением едкого натра. Образующийся при этом аммиак отгоняют в раствор кислоты и определяют его количество объемным методом.
Макрометод Кьельдаля
Ход анализа. 1. Окисление органического вещества почвы. Навеску почвы 3—10 г (в зависимости от предполагаемого содержания азота) помещают в колбу Кьельдаля емкостью 350 мл. Чтобы избежать при этом загрязнения горла колбы, навеску берут в пробирку. Нижний конец пробирки с помощью резиновой трубки присоединяют к стеклянной толстостенной трубке. Пробирку держат наклонно за трубку и на нее надевают колбу Кьельдаля так, чтобы открытый конец пробирки не достигал на 4—5 см до дна колбы. Колбу переворачивают и высыпают в нее почву. Туда же вносят 0,1 г порошка металлического селена и 8 г смеси сернокислого калия и медного купороса. Это делают с помощью небольшой воронки с длинным концом, опущенным на 2—3 см ниже начала расширяющейся части колбы. Мерным цилиндром туда же приливают 25 мл серной кислоты (уд. вес 1,83—1,84). Содержимое колбы тщательно перемешивают. Чтобы уменьшить или совсем исключить вспенивание жидкости при последующем нагревании, колбу оставляют при комнатной температуре на 3—4 часа (лучше на ночь). После этого содержимое ее нагревают при частом взбалтывании, регулируя нагрев, чтобы жидкость постепенно довести до кипения. Кипение продолжают несколько часов (3—5, а иногда и больше) в зависимости от содержания и качества органического вещества. Сжигание ведут под тягой. Его заканчивают, когда охлажденный раствор над осадком будет бесцветным или окрашенным в голубоватый цвет от присутствия меди.
Чтобы избежать выбрасывания раствора из колбы Кьельдаля во время кипения, особенно при толчках, которые могут возникнуть в конце сжигания, особенно при анализе песчаных почв, колбы устанавливают в наклонном положении на специальной металлической подставке. В процессе сжигания нагревают только ту часть колбы, где находится жидкость. Нагревание колбы выше уровня жидкости может привести к потерям азота.
Нагрев жидкости регулируют так, чтобы выделяющиеся при кипении пары серной кислоты концентрировались в горле колбы, примерно на 1/3 пути от его основания. При этом в колбе будет сохраняться необходимое количество серной кислоты. Улетучивание паров серной кислоты может привести к потерям азота из-за повышения температуры кипения жидкости в связи с увеличением концентрации сернокислого калия. Для предотвращения испарения серной кислоты можно использовать специальные пробки, которыми прикрывают колбы Кьельдаля. Пробки служат воздушными холодильниками и препятствуют испарению жидкости.
При большом содержании в почве карбонатов, чтобы избежать сильного вспенивания, серную кислоту приливают в колбу в несколько приемов, каждый раз взбалтывая ее содержимое. Следующую порцию кислоты приливают после прекращения бурного выделения CO2.
2. Отгон аммиака. Для отгона аммиака используют дистилляционные аппараты различных модификаций. В основе их лежит один принцип, различия лишь конструктивные. Наиболее удобны приборы с применением водяного пара.
Один из наиболее простых приборов для макроанализа показан на рис. 1. Он состоит из отгонной (дистилляционной) колбы 1 емкостью в 700—1000 мл (удобно использовать колбу Кьельдаля), соединенной при помощи шлифа с насадкой 2, в которую впаяна стеклянная трубка, одним концом доходящая почти до дна дистилляционной колбы, другим, снабженным воронкой 6 (закрывающейся стеклянной пробкой на шлифе), соединена шлифом или тефлоновой трубкой с ловушкой 8, присоединенной к парообразователю 7. Последним служит 3—5-литровая плоскодонная колба, на 2/3 заполняемая дистиллированной водой, доводимой до кипения. Ловушка внизу имеет кран, при помощи которого регулируется подача пара в дистилляционную колбу. Верхняя часть насадки 2 снабжена каплеуловителем 3, соединенным тефлоновой трубкой или шлифом с холодильником 4. Нижний конец холодильника оканчивается трубкой, которую опускают в приемник 5, представляющий собой плоскодонную или коническую колбу емкостью 400—500 мл. Во время работы холодильник обертывают полосками фильтровальной бумаги. Это предупреждает попадание в приемник капель, образующихся на наружных стенках холодильника в результате конденсации водяных паров из воздуха. Отгон аммиака проводят, пропуская водяной пар из парообразователя через исследуемый раствор, помещенный в дистилляционную колбу. Выделяющиеся при этом пары NH3 и воды, проходя через холодильник, конденсируются, и далее дистиллят поступает в приемную колбу. Чтобы избежать накопления в дистилляционной колбе большого количества жидкости в результате конденсации проходящего через раствор водяного пара, колбу подогревают, поддерживая раствор при слабом кипении. Перед работой воду в парообразователе слабо подкисляют серной кислотой для связывания могущего присутствовать в ней аммиака.
Полумикродистилляционный аппарат, недавно описанный Бремнером, для анализа почв показан на рис. 2. Этот прибор отличается высокой производительностью. Он удобен при отгоне аммиака, обогащенного 15N. Аппарат просто разбирается и благодаря этому стекло легко очищать от загрязнения тяжелым изотопом азота.
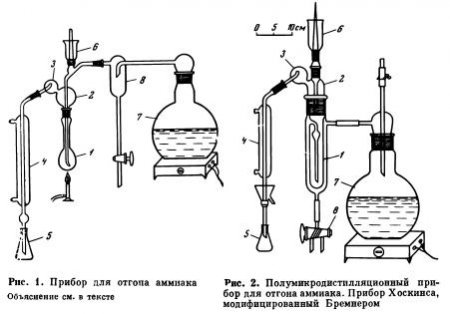
Прибор состоит из дистилляционного сосуда 1, снабженного кожухом, который внизу имеет трубку, соединенную с двухходовым краном 8. К одному отводу крана присоединяют водоструйный насос, с помощью которого освобождают дистилляционный сосуд после окончания анализа и при его промывании. Второй отвод крана служит для сообщения прибора с воздухом и спуска накапливающегося в кожухе конденсата водяных паров. К кожуху присоединен парообразователь 7. Последним служит 5-литровая плоскодонная колба. Верхняя часть дистилляционного сосуда при помощи широкого шлифа соединена с насадкой 2, снабженной каплеуловителем 3 и воронкой 6, закрывающейся стеклянной пробкой. Каплеуловитель соединен с холодильником 4. Нижний конец холодильника оканчивается трубкой, которую опускают в приемник 5, представляющий собой плоскодонную или коническую колбу емкостью 250 мл.
Чтобы избежать при проведении анализа попадания капель в приемник с поверхности холодильника (образующихся при конденсации водяных паров из воздуха), нижний конец холодильника снабжают воронкой, служащей для сбора и отвода конденсата. Парообразователь соединен с дистилляционным сосудом тефлоновой трубкой, остальные части прибора соединяются с помощью стеклянных шлифов.
Для обеспечения постоянного уровня воды в парообразователе в его пробку впаяна стеклянная трубка, подающая дистиллированную воду из резервуара, установленного выше парообразователя. Подачу воды регулируют зажимом. Воду в парообразователе слегка подкисляют серной кислотой для связывания могущего быть в ней аммиака. Для нагрева парообразователя используют газовые или электрические приборы. Пар, поступающий из парообразователя, прежде чем попасть в дистилляционный сосуд, нагревает его с наружной стороны. В связи с этим в дистилляционном сосуде не происходит конденсации большого количества водяного пара и уменьшается время отгона аммиака. Работая на двух приборах, один аналитик за рабочий день может отогнать 50—60 проб.
Если во взятой навеске почвы предполагают содержание азота больше 5 мг, то для отгона аммиака можно использовать только часть раствора, полученного после сжигания, применив полумикродистилляционный аппарат. Это занимает меньше времени и в случае необходимости позволяет повторить анализ. При меньшем содержании азота в навеске аммиак отгоняют из всего раствора, используя макроприбор.
Отгон NH3 из всего раствора. К содержимому колбы Кьельдаля, охлажденному до комнатной температуры после сжигания, осторожно (по стенкам) небольшими порциями при взбалтывании приливают 10—15 мл дистиллированной воды. Раствор с осадком переносят с помощью воронки в дистилляционную колбу макроприбора для отгона аммиака. Колбу Кьельдаля 4—5 раз ополаскивают водой по 40—50 мл, присоединяя ее к основному раствору. Если в колбе останется небольшое количество песка, его можно не переносить, достаточно только промывки водой. Присутствие песка в отгонной колбе может повлечь к возникновению толчков при дистилляции аммиака.
Раствору дают остыть, объем его доводят водой до 300—400 мл, после чего колбу присоединяют к прибору. В приемник наливают 10 мл 2 %-ного раствора борной кислоты, прибавляют 2—3 капли индикатора Гроака. Нижний конец отводной трубки холодильника погружают (примерно на 0,5—1 см) в раствор борной кислоты. Включают холодильник. Через воронку в дистилляционную колбу прибавляют 100 мл 40 %-ного раствора едкого натра. Затем, закрыв кран ловушки 8, сейчас же пускают пар из парообразователя, вода в котором предварительно должна быть доведена до кипения. Количество 40 %-ного раствора щелочи берут в 4 раза больше, чем концентрированной серной кислоты, взятой для сжигания.
Выделяющийся из раствора NH3 увлекается паром, который конденсируется, проходя через холодильник. Конденсат далее поступает в приемник, где NH3 поглощается кислотой. Ток водопроводной воды, охлаждающий холодильник во время отгона, регулируют, чтобы температура поступающего в приемник конденсата не превышала 25°. В начале отгона отводную трубку холодильника держат погруженной в раствор борной кислоты. Когда будут отогнаны основные количества аммиака (в приемнике накопится 100—150 мл раствора), дистилляцию продолжают, держа конец отводной трубки холодильника на 1—2 см выше уровня жидкости в приемнике. Отгон NH3 заканчивают, когда объем дистиллята достигнет 300—400 мл. Об этом судят по отсутствию реакции с реактивом Несслера в последних 2—3 мл дистиллята. По окончании отгона конец трубки холодильника ополаскивают водой, собирая ее в приемник, дистиллят титруют 0,02 н. раствором H2SO4. Окончание титрования устанавливают по переходу зеленой окраски в фиолетово-красную.
Аммиак образует с борной кислотой борат аммония по реакции
H3BO3 + 3NH4OH = (NH4)3BО3 + 3H2О.
При последующем титровании бората аммония раствором серной кислоты снова образуется борная кислота:
2(NH4)3BО3 + 3H2SO4 = 3 (NH4)2SO4 + H3BO3.
По количеству серной кислоты, пошедшей на титрование, рассчитывают содержание N — NH4 в растворе (1 мл 0,02н. H2SO4 соответствует 0,28 мг N).
Для связывания аммиака вместо борной кислоты можно использовать 0,02 н. титрованный раствор H2SO4. По окончании отгона избыток серной кислоты оттитровывают 0,02 н. раствором NaOH; по разности устанавливают количество связанного кислотой аммиака. Оба поглотителя по точности дают идентичные результаты. Однако применение борной кислоты более удобно, содержание N — NH4 устанавливают прямым титрованием, поэтому нет необходимости применять борную кислоту точной концентрации и точно отмеренного объема, не требуется титрованный раствор щелочи.
Чистоту реактивов проверяют холостым определением (проводят не менее двух определений). В колбу Кьельдаля помещают 25 мл концентрированной серной кислоты, туда же вносят K2SO4 и катализаторы в количествах, используемых при сжигании почвы. Смесь нагревают и кипятят 2 часа, далее проводят те же операции, что и при анализе почвы. Данные N — NH4 контрольного определения вычитают из результатов анализа почвы и рассчитывают содержание азота, выражая его в процентах от веса почвы.
Отгон NH3 из части раствора. Содержимое колбы Кьельдаля после сжигания навески охлаждают до комнатной температуры. В колбу небольшими порциями приливают 40—50 мл дистиллированной воды, каждый раз перемешивая раствор после добавления очередной порции. При этом часть осадка, находящегося на дне колбы, растворится, часть перейдет во взвешенное состояние. Если осадок трудно переходит в раствор, то колбу дополнительно подогревают. Раствор со взвесью при помощи небольшой воронки переносят в мерную колбу емкостью 250 мл. Колбу Кьельдаля несколько раз ополаскивают водой (по 20—30 мл), присоединяя промывные воды к основному раствору.
Для отгона NH3 применяют полумикродистилляционные приборы. Удобно использовать аппарат, показанный на рис. 2. При работе с ним в приемник наливают 5—10 мл 2 %-ного раствора борной кислоты, прибавляют 2—3 капли индикатора Гроака, нижний конец холодильника опускают в раствор борной кислоты. Кран 8 (см. рис. 2) ставят в положение, обеспечивающее доступ воздуха в прибор. Пипеткой из мерной колбы отбирают 30—50 мл раствора, полученного после сжигания почвы, его переносят в воронку прибора, вынимают пробку воронки. При этом раствор переходит в дистилляционный сосуд. Воронку ополаскивают небольшим количеством воды, закрывают пробкой. Затем в воронку помещают 40%-ный раствор NaOH, исходя из следующего расчета. Вычисляют, какое количество концентрированной серной кислоты, используемой для сжигания почвы, приходится на объем раствора, взятого для отгона; объем щелочи берут в 4 раза больше. Вынув пробку воронки, спускают раствор едкого натра в дистилляционный сосуд. Оставшуюся на воронке щелочь быстро смывают 10—15 мл воды, спуская ее в сосуд. Воронку сейчас же закрывают пробкой. Общее количество раствора в дистилляционном сосуде не должно превышать 80 мл (для определения его на сосуде при изготовлении ставят метку). В прибор подают пар из парообразователя, закрыв кран 8. Во время отгона регулируют интенсивность кипения воды в парообразователе, чтобы за 1 мин. в приемнике собиралось 5—6 мл дистиллята. Ток водопроводной воды, охлаждающий холодильник, должен обеспечивать температуру дистиллята не выше 25°. Когда в приемной колбе накопится 15—20 мл дистиллята, отгон продолжают, держа конец холодильника на 1—2 см выше уровня жидкости в приемнике. Отгон NH3 обычно заканчивается, когда в приемнике наберется 35 мл раствора (для удобства на колбе делают метку несмывающейся краской, указывающую нужный объем). Окончание дистилляции проверяют реактивом Несслера. Для этого конец холодильника обмывают водой (собирая ее в приемник), под него подставляют пробирку и, набрав 1—2 мл дистиллята, прибавляют 2—3 капли реактива Несслера. Отсутствие желтой окраски укажет на полноту отгона. Раствор в приемнике титруют 0,02 н. H2SO4, его окончание устанавливают по переходу зеленой окраски в фиолетовокрасную (1 мл 0,02 н. H2SO4 соответствует 0,28 мг N).
Холостое определение на чистоту реактивов проводят, как указано при описании отгона NH3 из всего раствора. Результаты холостого определения рассчитывают, исходя из общего количества раствора (до которого доведен раствор после сжигания) и объема его, взятого для отгона аммиака. Полученные величины вычитают из результатов анализа почв и рассчитывают содержание азота в процентах веса почвы.
Реактивы. 1. Концентрированная серная кислота (уд. вес. 1,83—1,84). Применяют х. ч. реактив. Серная кислота не должна содержать аммонийных солей и нитратов. Проверку ее на присутствие NH1 проводят следующим образом. К 15 мл дистиллированной воды приливают 1 мл серной кислоты. Жидкость охлаждают, нейтрализуют 10%-ным раствором едкого натра (в присутствии лакмусовой бумажки). Затем прибавляют еще 1 мл того же раствора щелочи и 0,5 мл реактива Несслера (приготовление см. ниже). Кислота пригодна при наличии слабо-желтой окраски раствора. Красно-бурая окраска раствора или [выпадение осадка указывают на большое содержание в кислоте аммонийных солей. Применяемые при испытании кислоты дистиллированная вода и щелочь не должны содержать аммония.
Испытание серной кислоты на присутствие нитратов проводят с хромотроповой кислотой. Растворяют 0,1 г динатриевой соли хромотроповой кислоты в 50 мл H2SO4. Для ускорения растворения раствор подогревают на водяной бане не более 3—4 мин. при температуре не выше 70°. Приобретение раствором желтой окраски указывает на присутствие нитратов в серной кислоте. Такая кислота не пригодна для работы.
2. 40%-ный раствор NaOH. В большой фарфоровой чашке растворяют 2,1 кг х. ч. едкого натра в 2 л воды. Содержимое чашки размешивают толстой стеклянной палочкой до полного растворения щелочи (при растворении едкого натра происходит разогревание раствора). Охлажденный до комнатной температуры раствор переносят в бутыль, закрывают резиновой пробкой. Через несколько дней прозрачный раствор над осадком сливают сифоном и объем его разводят в 2,5 раза дистиллированной водой, не содержащей углекислоты. Процентное содержание NaOH проверяют ареометром и, если требуется, раствор подгоняют до 40%-ного прибавлением воды (не содержащей CO2) или концентрированного раствора едкого натра. Если приготовленный реактив содержит аммиак (желтое окрашивание при прибавлении реактива Несслера), его удаляют кипячением раствора, используя для этого медную посуду (жидкость при этом приобретает голубой цвет от присутствия меди). После удаления аммиака раствор охлаждают и доводят водой, не содержащей углекислоты, до первоначального объема. Реактив хранят в склянке, закрытой резиновой пробкой.
3. Металлический селен (в порошке). Препарат может быть загрязнен солями аммония. Для очистки порошок промывают горячим раствором 0,5 н. KCl и затем водой для удаления избытка хлора (сначала горячей, затем холодной), высушивают на воздухе между листами фильтровальной бумаги.
4. Смесь сернокислого калия и сернокислой меди. На 10 частей х. ч. K2SO4 берут 1 часть CuSO4*5Н2O. Смесь растирают в фарфоровой ступке в тонкий порошок.
5. 0,02 н. титрованный раствор H2SO4.
6. Индикатор Гроака. Смешивают равные объемы 0,4%-ного спиртового раствора метилового красного и 0,2%-ного спиртового раствора метиленового синего. Хранят в темной склянке с притертой пробкой.
7. Реактив Несслера. Растворяют 25 г иодистого калия (KJ) в 30 мл воды, прибавляют 35 г иодистой ртути (красной) HgJ2 и в фарфоровой ступке пестиком растирают до полного растворения. Прибавляют 870 мл 15%-ного раствора КОН, перемешивают, дают отстояться и декантируют прозрачную жидкость. Раствор хранят в темной склянке.
Чтобы приготовить 15%-ный раствор КОН, 150 г едкого кали растворяют в 900—950 мл воды; после охлаждения доводят до 1 л водой.
В продаже имеется готовый реактив Несслера, им можно пользоваться при выполнении анализов.
8. Дистиллированная вода, применяемая при анализе и для приготовления реактивов, не должна давать реакцию на NH3 с реактивом Несслера.
Полумикрометод Кьельдаля
Ход анализа. Навеску почвы от 0,2 до 1 г (взвешенную с точностью 0,001 г) помещают в колбу Кьельдаля емкостью 50—100 мл. Туда же прибавляют 0,05 г Se, 1,5 г смеси K2SO4 и CuSO4, а также 5 мл серной кислоты (уд. вес 1,83—1,84). Содержимое колбы медленно доводят до кипения и продолжают его до обесцвечивания жидкости над осадком. После сжигания к раствору прибавляют 10 мл воды и количественно переносят в дистилляционный сосуд полумикродистилляционного аппарата. Далее в сосуд добавляют 20 мл 40 %-ного раствора NaOH и отгоняют NH3, предварительно налив в приемник 5 мл 2 %-ного раствора борной кислоты. Сжигание почвы и отгон NH3 проводят, соблюдая те же условия, что и при определении азота макрометодом. Приготовление реактивов описано там же.