Аминокислоты - производные глутаминовой кислоты (часть 1)
Глутаминовая кислота создает основу углеродного скелета для входящих в состав белка аминокислот глутамина, аргинина и пролина и небелковых аминокислот орнитина и цитруллина, важных промежуточных соединений на метаболических путях, ведущих к биосинтезу аргинина. Оксипролин, обнаруженный в нескольких растительных белках и играющий важную роль в биосинтезе клеточной стенки, образуется путем гидроксилирования остатков пролина после его включения в пептидную цепь.
Биосинтез пролина. Наиболее вероятный путь синтеза пролина в растительных клетках — в обход ацетилирования, по пути, на котором γ-карбоксильная группа глутамата реагирует с АТФ с образованием ацил фосфата, в свою очередь, восстанавливаемого НАДН до глутамат-γ-полуальдегида (рис. 2.4). Этот полуальдегид циклизуется в неферментативной реакции с потерей воды и образованием Δ'-пирролин-5-карбоновой кислоты, которая в заключение восстанавливается НАДН до пролина.
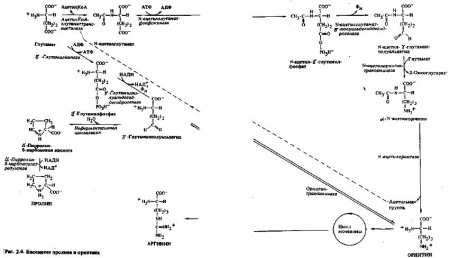
Биосинтез аргинина. В качестве промежуточных метаболитов в синтезе аргинина участвуют ацетилированные производные глутамата (рис. 2.4). Блокирование аминогруппы глутамата перед восстановлением до полуальдегида препятствует осуществлению той циклизации, которая происходит при образовании пролина, и делает возможным переаминирование γ-альдегидной группы с аминогруппой, в результате чего после удаления блокирующей ацетильной группы образуется небелковая аминокислота орнитин. Большинство растений в состоянии использовать в качестве доноров ацетильной группы при образовании N-ацетилглутамата как ацетилКоА, так и N-ацетилорнитин, в результате ацетилКоА используется в самом начале этого пути, затем ацетильная группа сохраняется благодаря тому, что интермедиат пути N-ацетилорнитин служит донором ацетильной группы в последующих реакциях ацетилирования, ведущих к образованию N-ацетилглутамина и орнитина (рис. 2.4). В реакции переаминирования на пути от N-ацетилглутамата к орнитину необычно участие альдегидной, а не оксогруппы.